Генномодифицированная рыба фото
Генетически модифицированный лосось в Канаде
Базирующаяся в штате Массачусетс компания AquaBounty Technologies объявила, что продала первые 10000 фунтов (4535 кг) генетически модифицированного лосося своим клиентам в Канаде. Цена рыбы составила 5,30 доллара за фунт (0,45 кг).
 © Paul Darrow/NYT/Redux/eyevine
© Paul Darrow/NYT/Redux/eyevine
Генетически модифицированные лососи были выращены AquaBounty Technologies в рыбоводном хозяйстве на маленьком острове у берегов Панамы. В ближайшем будущем компания планирует расширить производство и создать рыбозавод на острове Принца Эдуарда в Канаде, где уже получено разрешение местных властей на строительство. Также компания приобрела рыбозавод в Олбани (штат Индиана) и ведет переговоры с регулирующими органами США.
Этому событию предшествовала длинная, упорная борьба за признание генномодифицированного лосося регулирующими органами. «Кто-то должен быть первым, и я рад, что это были они, а не я, – признается генетик из Университета Вандербильта в Нэшвилле, который стал соучредителем стартап-компании AgGenetics, работающей с коровами. – Если бы они потерпели неудачу, это могло бы убить инженерную животноводческую отрасль на протяжении целого поколения».
Ученые впервые продемонстрировали генетически модифицированного лосося еще в 1989 годы. В 1990-е для совершенствования этой рыбы и ее коммерческого производства была создана AquaBounty Technologies. Тогда эта компания потратила 60 млн. долларов на внедрение в геном атлантического лосося (Salmo salar) гена чавычи (Oncorhynchus tshawytscha), ответственный за гормон роста, и генетических регуляторных элементов американской бельдюги (Zoarces americanus). Целью было добиться более быстрого роста рыбы. Модифицированные лососи достигают товарного размера примерно за 16 – 18 месяцев (обычный атлантический лосось – за три года). Полученная разновидность получила название AquAdvantage salmon. Модифицированные лососи триплоидные (их клетки содержат утроенный набор хромосом). Для коммерческого производства выращивают только самок, которые из-за индуцированной триплоидии почти все стерильные (98,9 %), что уменьшает риск скрещивания их с дикими лососями, если вдруг AquAdvantage salmon попадет в дикую природу.
Но фирме пришлось ждать четверть века пока Управление по контролю качества пищевых продуктов и лекарственных препаратов США (FDA) рассматривала более 50 исследований, демонстрирующих, что такой лосось не несет никаких угроз. В сентябре 2010 года консультативная группа FDA указала, что рыба «с очень малой вероятностью может оказать какие-либо значительные воздействия на окружающую среду» и что в качестве пищи она «столь же безопасна, как и обычный атлантический лосось». Тем не менее, в октябре того же года группа законодателей обратилась в FDA с требованием отклонить заявку. Дальнейшие обсуждения и повторные экспертизы растянулись еще на десять лет. 19 ноября 2015 года FDA наконец одобрило рыбу. За время пока тянулось рассмотрение, AquaBounty Technologies успела вырастить десять поколений своих лососей.
Министерство окружающей среды Канады еще в 2013 году одобрило икру модифицированных лососей для продажи на территории страны. В мае 2016 года канадское агентство по надзору за пищевыми продуктами (CFIA) разрешило продавать и самих рыб.
А вот в США продажа лососей так пока не начата, поскольку закон, определяющий бюджет США на 2017 год, включает пункт с требованием, чтобы FDA запретило продажу генноинженерных лососей, пока не будет разработана программа информирования потребителей об особенностях товара.
Часть американских политиков к лососям от AquaBounty Technologies относится и вовсе неодобрительно. Сенатор-республиканец от штата Аляска Лиза Мурковски назвала такого лосося «поддельной рыбой». Как в США, так и в Канаде ряд активистов требовали пересмотреть решения регулирующих органов и даже подали судебные иски. Одна из таких общественных групп Центр безопасности пищевых продуктов (Center for Food Safety) в Вашингтоне утверждает, что FDA не имеет юридических полномочий для контроля над генетически модифицированными животными и что FDA приняла свое решение без полного учета потенциальных экологических рисков. Ряд торговых сетей США (Whole Foods, Trader Joe’s, Aldi) заявляют, что в их магазинах модифицированный лосось не появится.
Генеральный директор компании Рон Стотиш (Ron Stotish) говорит, что генноинженерные лососи выращиваются в закрытых емкостях, не имеющих связи с океаном. Это защищает лососей от многих патогенов и паразитов, с которыми сталкиваются их сородичи в природной среде. Также Стотиш отмечает, что генетически модифицированные рыбы экономически перспективны не только из-за своего быстрого роста, но и из-за того, что их можно выращивать вблизи больших городов, а не привозить издалека (сейчас большинство лососей, продаваемых в магазинах США, завозится из Норвегии или Чили).
Эра генетически модифицированных животных (2 фото)

Рыба, комары, коровы… На животных уже проводится множество генетических испытаний для повышения эффективности скотоводства и создания новых медикаментов.
Генетически модифицированные растения сегодня выращивают на 175 миллионах гектаров по всему миру (13% всех возделываемых площадей). Появляются они и в Европе: с апреля 2015 года в ЕС разрешил ввоз и продажу 17 типов ГМО.
Скоро наступит черед животных? Хотя опыты в области животной генной инженерии проводятся с 1980-х годов, пока что все еще находится на стадии исследований. Как бы то ни было, сейчас появляется все больше примеров конкретного применения полученных знаний. Рушатся последние технологические барьеры, которые не давали человеку испробовать любые возможные сочетания генов.
Бельгийская модифицированная порода коров


Процесс сродни селекции
Человек меняет гены животных на протяжение столетий. «Мы всего лишь называли эту практику селекцией», — объясняет генетик Марк Вестхузин. Если несколько поколений скрещивать одну породу собак с другой, в результате получится генетический коктейль, который природа вряд ли бы смешала сама — это болонка.
Новые генетические инструменты позволяют сделать изменения точнее и быстрее. «Мы меняем черты более точечным образом: мы можем точно сказать, что создаем», — объясняет Элисон Ван Эрнам, специалист по геному и биотехнологиям из Калифорнийского университета.
Первым животным, чей геном подвергся изменениям в лабораторных условиях, стала мышь. В 1982 году ученым удалось создать мышь, организм которой выделял значительное количество гормонов роста. И та достигла размеров небольшой крысы.
Лечение трансгенным молоком
Животное выросло вдвое больше нормальных размеров? Этой научной находке есть чем заинтересовать сельское хозяйство. В два раза больший лосось уже был выведен (коммерческое название AquAdvantage) и может стать первой генетически модифицированной рыбой, которую будут продавать для употребления в пищу. Компания ждет лишь отмашки американских властей.
Кроме того, животные могут получить иммунитет от эпидемий. Так, например, британские генетики вывели курицу, которой не страшен птичий грипп. В Бразилии генетически модифицированных комаров используют для борьбы с лихорадкой денге.
Что еще интереснее, молоко трансгенных животных таит в себе безграничные возможности. Коров уже меняли для получения материнского и гипоаллергенного молока (для тех, у кого имеется непереносимость лактозы). В будущем же можно будет получить молоко с человеческими антителами для борьбы с меланомой.
Американская компания GTC Biotherapeutics вывела коз, чье молоко содержит антитромботические вещества: получивший название ATryn предотвращает возникновение кровяных сгустков.
Вариантов скрещивания генов существует множество, и некоторые из них весьма необычны: после испытания на козах бактерии изменили для выработки паутины. Этот материал (считается самым прочным в мире) позволил бы создать сверхэффективные пуленепробиваемые жилеты и медицинские ткани.
Рыбам-зебрам же досталась ДНК светящейся медузы. Цель эксперимента: заставить их светиться в присутствии определенных токсинов для выявления загрязнения воды.
Как бы то ни было, GloFish снискали больше успеха в аквариумах американцев, став первым генетически модифицированным домашним животным.
Генетические «скальпели»
Ученые продвигаются все дальше и дальше в расшифровке генома. Речь идет о понимании того, как тот или иной ген определяет характеристики вида. Прогресс в генетике ускорился еще больше с обнаружением новых эффективных инструментов, в первую очередь Cas9.
Техника Cas9 была «случайно» открыта учеными Эмманюэль Шарпантье и Дженнифер Дудной в ходе опытов на вирусах. Если не вдаваться в подробности, она позволяет найти определенный участок ДНК и вырезать его. При добавлении другого материала она также дает возможность заменить его иным участком ДНК.
По словам Дженнифер Дудны, все это стало большим шагом вперед:
«Если в прошлом технологии были подобны кузнечному молоту, сейчас мы работаем с геномом молекулярными скальпелями».
Возрождение мамонтов и динозавров
Имея на руках подобные технологии, некоторые ученые собираются возродить исчезнувшие виды или даже создать новые.
В теории ученые уже понимают, как можно было бы вернуть к жизни исчезнувшего 10 тысяч лет назад шерстистого мамонта: благодаря найденным во льдах тканям и кусочкам зубов им удалось практически полностью воссоздать его геном. Остается лишь изменить гены слона или вживить его ДНК в яйцеклетку слонихи, чтобы на свет появился маленький мамонт.
А что насчет динозавров? Раз курица — потомок некоторых из них, всего лишь достаточно обратить процесс вспять… Ученые уже проделали это и смогли реактивировать древние «динозаврьи» гены курицы.
Голые модифицированные куры



Из-под генетического скальпеля на свет могли бы выйти мифические или даже абсолютно фантастические существа. Американский палеонтолог Джек Хорнер говорил о возможности создать единорога.
Как бы то ни было, вывести животных необычных размеров (утку размером с лошадь или лошадь размером с утку) представляется нетривиальной задачей: рост определяется сотнями генов. То же самое касается и крылатых свиней. Ученые не видели позвоночных с шестью конечностями, и понятия не имеют, на что был бы похож их генетический код.
Как далеко можно зайти?
Но куда могут привести подобные манипуляции с геномом? Научная фантастика на свой манер уже не раз предупреждала человечество об опасностях таких экспериментов. Вспомните хотя бы эту цитату из «Парка Юрского периода»:
«Наши ученые так сосредоточились на том, что они могли сделать, что даже не задумались, было ли у них на то право».
Если отойти в сторону от причудливых генетических созданий, трансгенные изменения животных для повышения качества и производительности могли бы обеспечить продовольственную безопасность по всему миру. Но какими были бы долгосрочные последствия? Экологические и санитарные риски? Лосось AquAdvantage еще даже не появился на наших тарелках, но уже вызывает опасения насчет «генетического загрязнения».
Хотя пока что никто не в силах ответить на эти вопросы, нам давно пора очертить этические пределы: как стало известно, китайские ученые начали менять человеческий геном.
Генетически модифицированные животные (12 фото)
Далее мы поговорим о том, что так сильно пугает многих людей, общественных и религиозных деятелей, а также политиков – генетической модификации организмов (ГМО). Мы расскажем вам о том, кто, как и для чего модифицирует животных.
Комбинированная фотография, показывающая клонированного флюоресцирующего щенка, трехмесячной гончей, под ультрафиолетовым светом (слева) и под обычной лампой, май 2009 года. Это представитель второго поколения генетически модифицированных собак в Ветеринарном колледже Сеульского национального университета, доказательство возможности передачи флюоресцирующих генов от матери к потомству. Флюоресцирующий ген был получен путем впрыскивание соответствующего белка, взятого из рыбок, в клетки собаки.
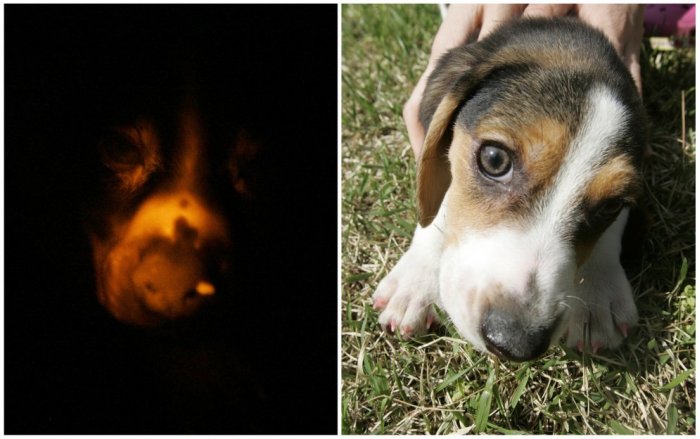

Все представители второго поколения.


Афганская борзая по кличке Снуппи — первая в мире клонированная собака, отдыхает во время фотосессии в Ветеринарном колледже Сеульского национального университета, 12 марта 2008 года. Южнокорейская биотехнологическая компания, созданная выходцами из учебного заведения, предлагает владельцам собак шанс на успешное клонирование их любимца за сумму порядка 140 тыс. долларов СШАС. Снуппи стал первой в мире собакой, для клонирования которой успешно применили метод “терапевтического клонирования” — перенос ядра соматической клетки с целью получения линий эмбриональных стволовых клеток с геномом исходной соматической клетки, позволяющую получать иммунологически совместимый клеточный материал.


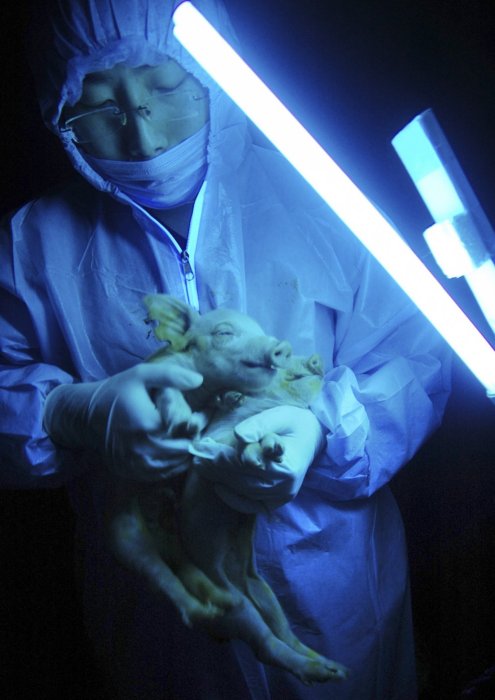
Две трансгенные свиньи в ультрафиолетом изучении, так что видна зеленая флуоресценция, специальный белок-маркер. Свинарник в Харбине, на северо-востоке Китая, 26 декабря 2006 года. Это первые в Китае успешно генетически модифицированные свиньи.

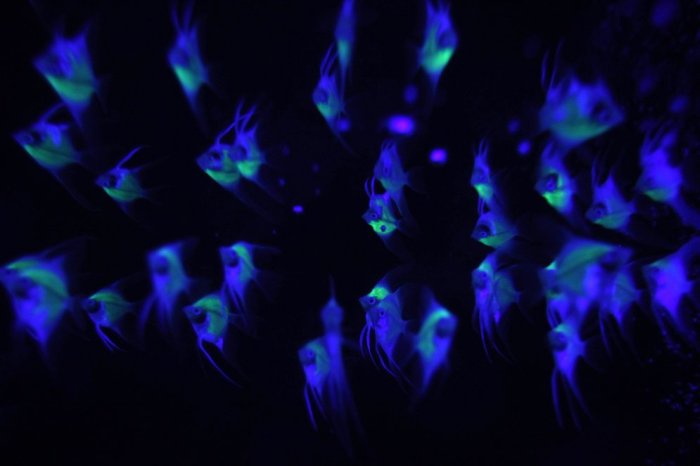
Генетически созданная коралловая рыбка (Pterophyllum) светится в аквариуме во время научной конференции Taiwan International Aquarium Expo 2012 в Тайпее. Она считается первой в мире флюоресцирующей рыбкой, чей фиолетовый цвет виден без специальной лампы с “черным светом” (ультрафиолетовая лампа с минимальным видимым спектром излучения). Создатели рыбки — тайваньскаяAcademia Sinica, National Taiwan Ocean University и частная биотехнологическая компания Jy Lin.


Такие же рыбки, но в большом количестве.

Биолог помещает свою руку в ящик с самцами москитов Aedes aegypti на образовательной выставке, организованной в Бразилии британской биотехнологической компанией Oxitec, 5 марта 2015 года. Компания создала москитов “мужского пола”, которые “запрограммированы” на уничтожение своего потомства после спаривания с дикими самками. Эти насекомые будут отпущены в дикую природу — так правительство Бразилии надеется уменьшить количество насекомых этого вида, которые являются разносчиками возбудителей лихорадки денге. Только за два месяца этого года в Бразилии этой лихорадкой заболели более 100 тыс. человек.


Ноори, клонированная кашмирская коза, “носительница” одноименной и чрезвычайно редкой шерсти, созданная в региональном университете. Для жителей Кашмира обработка шерсти всегда была основным бизнесом, но в последнее время он страдает под натиском дешевых подделок. Клонирование лучших представителей породы может поспособствовать увеличению популяции и снижению цены на оригинальную кашмирскую шерсть.


Пенг-пенг, ягненок, которого китайские учены клонировали, взяв за основу генетически модифицированную овцу с “хорошими жирами”, обычно содержащимися в орехах, семенах, рыбе и зеленолистных овощах. Повсеместное разведение подобных овец могло бы сделать баранину чрезвычайно полезным мясом. Фотография сделана в марте 2012 года в лаборатории на востоке Китая.


Южнокорейский ученый Хван У Сок и его команда дарят представителям регионального правительства восьмерых клонированных койотов, принадлежащих к вымирающему виду — в надежде сохранить популяцию. Октябрь 2011 года. Хван У Сок, бывший профессор териогенологии и биотехнологии в Сеульском национальном университете, печально известен как автор серии поддельных экспериментов в области исследования стволовых клеток.


Генетически модифицированная собака Тагон и ее потомство, созданные в Ветеринарном колледже Сеульского национального университета, 2011 год. Южнокорейские ученые создали светящуюся собаку, которая может помочь в поиске лекарств от таких человеческих болезней, как Альцгеймер и Паркинсон. Тагон и все ее потомство содержат ген, вызывающий свечение в ультрафиолетовом излучении. Получение с пищей определенных веществ может “включать” и “выключать” это свечение, что дает ученым возможность экспериментировать на живом организме, получая быстрые, наглядные и однозначные результаты — это в разы ускоряет ход поиска новых лекарств для людей.
Генномодифицированная рыба фото
Войти
Генетически модифицированные домашние животные
Трансгенные животные давно покинули пределы лабораторий и постепенно приходят к нам в дом. Ученым эти животные помогают находить противоядия против ВИЧ и птичьего гриппа, сельскому хозяйству — увеличивать прирост мышечной массы, а людям — получать забавных зверушек. Кому и зачем нужны флуоресцирующие сердца трансгенных свиней, кошачий СПИД и собаки-халки — рассказывает в этой галерее.
На изображении — два куриных птенца. У того, что слева, флуоресцентный белок, поэтому у него под действием ультрафиолета светятся клюв и лапки. Правительство Великобритании поддержало работы по выведению таких птенцов с целью борьбы с птичьим гриппом. Только в 2015 году от этого заболевания в США погибли более 48 миллионов кур и индеек. Излучение позволяет ученым Кембриджского и Эдинбургского университетов отличить обычных птиц от генномодифицированных, в организме которых тормозится размножение и активность вируса птичьего гриппа. Модифицированные куры оказались менее восприимчивыми и к другим видам инфекции. Ученые обещают, что не всех генетически измененных животных будущего сделают светящимися.
Американские ученые из частной клиники Мейо в Рочестере использовали кошек для борьбы со СПИДом. В исследовании, результаты которого опубликованы в журнале Nature Methods, авторы использовали гены обезьян, которые блокировали FIV (Feline Immunodeficiency Virus, вируса кошачьего иммунодефицита) — аналог ВИЧ (Human Immunodeficiency Virus, вируса человеческого иммунодефицита). Модифицированным кошкам внедряли гены медузы Aequorea victoria, из-за которых животные светились. Тесты на клетках, полученных от необычных кошек, демонстрировали устойчивость к FIV. Пути распространения, проявление, течение и последствия воздействия этого вируса на организмы кошек и человека схожи, однако кошки редко умирают от FIV. Этот вирус безвреден для человека, как и ВИЧ — для кошек. Ученые оптимистично настроены и надеются бороться с FIV (а значит — и с ВИЧ: ДНК людей и кошек совпадают примерно на 90 процентов) при помощи генной терапии.
Ученые из Тайваньского национального университета вырастили светящихся в темноте зеленым светом трансгенных свиней. Исследователи утверждают, что в отличие от других ученых им впервые удалось вырастить животных, внутренние органы которых (в частности, сердце) тоже светятся. При дневном свете у свиней глаза, зубы и кожа имеют зеленоватый оттенок. Как и кошкам, животным ввели генетический материал медуз. Специалисты полагают, что такие свиньи стимулируют исследования стволовых клеток и помогут с изучением заболеваний человека. По словам ученых, кроме того, что животные светятся в темноте, они ничем не отличаются от обычных свиней.
Пекинский институт геномики изначально создал микросвиней для исследований заболеваний человека. Теперь ученые собираются продавать свинок, размеры которых не превышают габаритов небольшой собаки, по 1,6 тысячи долларов за особь. Такой поросенок весом не более 15 килограммов может стать отличным домашним питомцем. Предки микросвинок были как минимум в три раза тяжелее. Китайские ученые в сотрудничестве с европейскими коллегами выключили часть генов, ответственных за рост организма. Впрочем, не все ученые согласны с тем, что трансгенные свинки имеют право становиться домашними животными. По их мнению, это может негативно сказаться на восприятии в обществе генетики и трансгенных продуктов.
Собаки Геркулес (слева) и Тяньгоу
Ученые из Гуанчжоу вывели собак со сверхмощной мускулатурой. Генетики удалили у подопытных биглей ген, отвечающий за выработку миостатина — белка, подавляющего рост и дифференцировку мышечной ткани. Его блокирование приводит к значительному увеличению сухой мышечной массы с практически полным отсутствием жировой ткани. В результате у собак в два раза более мощная мускулатура, чем у их сородичей, и они более выносливы. Ученые собираются использовать собак для исследований появления и протекания болезни Альцгеймера.
В отличие от Геркулеса и Тяньгоу, мышечная масса уиппета по кличке Большая Венди обусловлена природной генетической мутацией, также связанной с выработкой миостатина. Масса собаки-халка превышает 27 килограммов — в два раза больше нормы, однако размеры головы, сердца, легких и ног этого уиппета такие же, как у обычных представителей этой породы.
Мускулистая собака породы грейхаунд по кличке Салли
Бельгийская голубая корова
Бельгийская голубая корова выводилась селекционерами в период с 1920-го до 1950 года. Ученые и фермеры отдавали предпочтение животным с большой мышечной массой, а не тем, которые давали много молока. Быки этой породы могут иметь массу более 1,3 тонны и достигать 1,5 метра в высоту. Мышцы у таких животных появляются на шестой неделе от рождения и дают на выходе до 80 процентов больше мяса по сравнению с обычными коровами. У бельгийских голубых также наблюдаются мутации, связанные с выработкой миостатина.
Флуоресцирующая тернеция GloFish
Компания GloFish продает разноцветных светящихся рыбок. Зеленые содержат ген медузы Aequorea Victoria, а красные — коралла рода Discosoma. Рыбки с двумя генами имеют желтый цвет. Компания запатентовала свой бренд, а ее рыбки стали первыми общедоступными генномодифицированными домашними питомцами.
Конечно, не обошлось и без мышей. На фото особи со светящимися зеленым хвостами, ушами, глазами, носами и лапками. Этим животным ввели флуоресцентный ген GFP, впервые выделенный из ДНК морской медузы в 1994 году. За это в 2008 году ученым Мартину Чалфи, Осаму Симомуре и Роджеру Тьсену присудили Нобелевскую премию по химии.
via